Examen histopatológico de la efectividad de los aloinjertos óseos no vascularizados de tibia y fémur en la curación ósea en fracturas de tibia de rata
Resumen
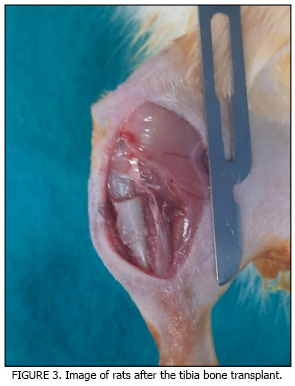
El objetivo de este estudio fue evaluar histológicamente el proceso de curación de fracturas de tibia reconstruidas con injertos óseos alogénicos procedentes de diferentes regiones anatómicas (tibia y fémur). Se utilizaron veinticinco ratas Sprague-Dawley, divididas en cuatro grupos: control de fractura (n = 7), trasplante óseo alogénico de tibia (n = 7), trasplante óseo alogénico de fémur (n = 7) y grupo donante (n = 4). Bloques de hueso corticocanceloso (5×5 mm) obtenidos de los animales donantes se fijaron a los focos de fractura creados en las tibias de las ratas receptoras mediante agujas de Kirschner. Tras un periodo de curación de cuatro semanas, se sacrificaron las ratas y se examinaron histológicamente las tibias. Las muestras de tejido se fijaron en formalina neutra al 10 %, se descalcificaron, se incluyeron en parafina y se tiñeron con hematoxilina-eosina. La tasa de formación de hueso nuevo se evaluó histomorfométricamente y se analizó mediante la prueba de Kruskal-Wallis. Se observó formación de callo óseo en la línea de fractura en todos los grupos. El tejido calloso fue más uniforme y la formación de hueso nuevo más densa en los grupos de trasplante alogénico de tibia y fémur. La mayor formación de hueso nuevo se observó en el grupo de trasplante de hueso alogénico de tibia y fémur en comparación con los controles (P < 0,05; P = 0,002). El trasplante de hueso alogénico no vascularizado, mediante injertos derivados de tibia y fémur, incrementó significativamente la consolidación de la fractura en comparación con el grupo control. Se concluyó que el uso de hueso alogénico obtenido de diferentes sitios anatómicos puede ser una opción eficaz y biocompatible para la regeneración ósea.
Descargas
Citas
Lelo I, Calabrese G, De Luca G, Conoci S. Recent Advances in Hydroxyapatite-Based Biocomposites for Bone Tissue Regeneration in Orthopedics. Int. J. Mol. Sci. [Internet]. 2022; 23(17):9721. doi: https://doi.org/g8rzn6 DOI: https://doi.org/10.3390/ijms23179721
Sun J, Xie W, Wu Y, Li Z, Li Y. Accelerated Bone Healing via Electrical Stimulation. Adv. Sci. [Internet]. 2025; 12(24):e2404190. doi: https://doi.org/g8694w DOI: https://doi.org/10.1002/advs.202404190
Omi M, Mishina Y. Roles of osteoclasts in alveolar bone remodeling. Genesis. [Internet]. 2022; 60(8-9):e23490. doi: https://doi.org/gtz76m DOI: https://doi.org/10.1002/dvg.23490
Maruyama M, Rhee C, Utsunomiya T, Zhang N, Ueno M, Yao Z, Goodman SB. Modulation of the inflammatory response and bone healing. Front. Endocrinol. [Internet]. 2020; 11:386. doi: https://doi.org/gjtsz6 DOI: https://doi.org/10.3389/fendo.2020.00386
Moriarty TF, Metsemakers WJ, Morgenstern M, Hofstee MI, Vallejo-Diaz A, Cassat JE, Wildemann B, Depypere M, Schwarz EM, Richards RG. Fracture-related infection. Nat. Rev. Dis. Primers. [Internet]. 2022; 8(1):67. doi: https://doi.org/mq9t DOI: https://doi.org/10.1038/s41572-022-00396-0
Steppe L, Megafu M, Tschaffon-Müller ME, Ignatius A, Haffner-Luntzer M. Fracture healing research: Recent insights. Bone Rep. [Internet]. 2023; 19:101686. doi: https://doi.org/g4nz6p DOI: https://doi.org/10.1016/j.bonr.2023.101686
Shu LZ, Zhang XL, Ding YD, Lin H. From inflammation to bone formation: the intricate role of neutrophils in skeletal muscle injury and traumatic heterotopic ossification. Exp. Mol. Med. [Internet]. 2024; 56(7):1523-30. doi: https://doi.org/g8xfdh DOI: https://doi.org/10.1038/s12276-024-01270-7
Camarena A, Kang L, Mirando AJ, Augustine E, McMillian NS, Stinson NC, Agarwal SM, Becker ML, Hilton MJ, Fernandez-Moure JS. Platelet-rich plasma enhances rib fracture strength and callus formation in vivo. J. Trauma Acute Care Surg. [Internet]. 2024; 97(6):884-890. doi: https://doi.org/qmx3 DOI: https://doi.org/10.1097/TA.0000000000004441
Trompet D, Melis S, Chagin AS, Maes C. Skeletal stem and progenitor cells in bone development and repair. J. Bone Miner. Res. [Internet]. 2024; 39(6):633-654. doi: https://doi.org/gt2h8d DOI: https://doi.org/10.1093/jbmr/zjae069
Hente RW, Perren SM. Tissue deformation controlling fracture healing. J. Biomech. [Internet]. 2021; 125:110576. doi: https://doi.org/qmx4 DOI: https://doi.org/10.1016/j.jbiomech.2021.110576
Wang YH, Zhao CZ, Wang RY, Du QX, Liu JY, Pan J. The crosstalk between macrophages and bone marrow mesenchymal stem cells in bone healing. Stem Cell Res. Ther. 2022; 13(1):524. doi: https://doi.org/qscv DOI: https://doi.org/10.1186/s13287-022-03211-5
ZhaoQ, Liu X, Yu C, Xiao Y. Macrophages and Bone Marrow-Derived Mesenchymal Stem Cells Work in Concert to Promote Fracture Healing: A Brief Review. DNA Cell Biol. [Internet]. 2022; 41(3):276-284. doi: https://doi.org/grs8x6 DOI: https://doi.org/10.1089/dna.2021.0869
Rodríguez-Merchán EC. A Review of Recent Developments in the Molecular Mechanisms of Bone Healing. Int. J. Mol. Sci. [Internet]. 2021; 22(2):767. doi: https://doi.org/gscc6q DOI: https://doi.org/10.3390/ijms22020767
Bingül MB, Gül M, Dundar S, Tanik A, Artas G, Polat ME. Enhanced Bone Healing Through Systemic Capsaicin Administration: An Experimental Study on Wistar Rats. Med. Sci. Monit. [Internet]. 2024; 30:942485. doi: https://doi.org/qscw DOI: https://doi.org/10.12659/MSM.942485
Miron RJ. Optimized bone grafting. Periodontol. 2000. [Internet]. 2024; 94(1):143-160. doi: https://doi.org/g9dx5s DOI: https://doi.org/10.1111/prd.12517
Sanz-Sánchez I, Sanz-Martín I, Ortiz-Vigón A, Molina A, Sanz M. Complications in bone-grafting procedures: Classification and management. Periodontol. 2000. [Internet]. 2022; 88(1):86-102. doi: https://doi.org/gts4dr DOI: https://doi.org/10.1111/prd.12413
Schmidt AH. Autologous bone graft: Is it still the gold standard? Injury. [Internet]. 2021; 52(2):18-22. doi: https://doi.org/gnn7qp DOI: https://doi.org/10.1016/j.injury.2021.01.043
Zhao R, Yang R, Cooper PR, Khurshid Z, Shavandi A, Ratnayake J. Bone Grafts and Substitutes in Dentistry: A Review of Current Trends and Developments. Molecules. [Internet]. 2021; 26(10):3007. doi: https://doi.org/gsmsrh DOI: https://doi.org/10.3390/molecules26103007
Goutam M, Batra N, Jyothirmayee K, Bagrecha N, Deshmukh P, Malik S. A comparison of xenograft graft material and synthetic bioactive glass allograft in immediate dental implant patients. J. Pharm. Bioallied Sci. [Internet]. 2022; 14(1):980-982. doi: https://doi.org/qscz DOI: https://doi.org/10.4103/jpbs.jpbs_808_21
Ferraz MP. Bone Grafts in Dental Medicine: An Overview of Autografts, Allografts and Synthetic Materials. Materials. [Internet]. 2023; 16(11):4117. doi: https://doi.org/ DOI: https://doi.org/10.3390/ma16114117
Lee SS, Huber S, Ferguson SJ. Comprehensive in vitro comparison of cellular and osteogenic response to alternative biomaterials for spinal implants. Mater. Sci. Eng. C. [Internet]. 2021; 127:112251. doi: https://doi.org/qsc2 DOI: https://doi.org/10.1016/j.msec.2021.112251
Stopa Z, Siewert-Gutowska M, Abed K, Szubinska-Lelonkiewicz D, Kaminski A, Fiedor P. Evaluation of the safety and clinical efficacy of allogeneic bone grafts in the reconstruction of the maxilla and mandible. Transplant. Proc. [Internet]. 2018; 50(7):2199-2201. doi: https://doi.org/gfchtk DOI: https://doi.org/10.1016/j.transproceed.2018.02.122
Ippolito JA, Martinez M, Thomson JE, Willis AR, Beebe KS, Patterson FR, Benevenia J. Complications following allograft reconstruction for primary bone tumors: Considerations for management. J. Orthop. [Internet]. 2019; 16(1):49-54. doi: https://doi.org/gj33n7 DOI: https://doi.org/10.1016/j.jor.2018.12.013
Zou W, Li X, Li N, Guo T, Cai Y, Yang X, Liang J, Sun Y, Fan Y. A comparative study of autogenous, allograft and artificial bone substitutes on bone regeneration and immunotoxicity in rat femur defect model. Regen. Biomater. [Internet]. 2020; 8(1):40. doi: https://doi.org/qsc9 DOI: https://doi.org/10.1093/rb/rbaa040
Ciszynski M, Dominiak S, Dominiak M, Gedrange T, Hadzik J. Allogenic Bone Graft in Dentistry: A Review of Current Trends and Developments. Int. J. Mol. Sci. [Internet]. 2023; 24(23):16598. doi: https://doi.org/qqcn DOI: https://doi.org/10.3390/ijms242316598
Baldwin P, Li DJ, Auston DA, Mir HS, Yoon RS, Koval KJ. Autograft, Allograft, and Bone Graft Substitutes: Clinical Evidence and Indications for Use in the Setting of Orthopaedic Trauma Surgery. J. Orthop. Trauma. [Internet]. 2019; 33(4):203-213. doi: https://doi.org/gmtzbb DOI: https://doi.org/10.1097/BOT.0000000000001420
Sheen JR, Mabrouk A, Garla VV. Fracture healing overview. In: StatPearls. [internet]. Treasure Island, FL: StatPearls Publishing. 2023 [20 Aug 2025]. Available in: https://goo.su/qx3Z
Pajarinen J, Lin T, Gibon E, Kohno Y, Maruyama M, Nathan K, Lu L, Yao Z, Goodman SB. Mesenchymal stem cellmacrophage crosstalk and bone healing. Biomaterials. [Internet]. 2019; 196:80-89. doi: https://doi.org/gh4vp4 DOI: https://doi.org/10.1016/j.biomaterials.2017.12.025
Tanrisever M, Tekin B, Can UK, Istek O, Ozcan EC, Ozercan IH, Gelic T, Dundar S. The Effect of Local Melatonin Application on Bone Fracture Healing in Rat Tibias. Medicina. [Internet]. 2025; 61(1):146. doi: https://doi.org/qmzf DOI: https://doi.org/10.3390/medicina61010146
Ciobanu P, Danciu M, Pascu A, Gardikiotis I, Forna N, Sirbu MT, Calistru AE, Puha B, Veliceasa B, Sirbu PD. Experimental Study on Rats with Critical-Size Bone Defects Comparing Effects of Autologous Bone Graft, Equine Bone Substitute Bio-Gen® Alone or in Association with Platelet-Rich Fibrin (PRF). Polymers. [Internet]. 2024; 16(11):1502. doi: https://doi.org/qsdb DOI: https://doi.org/10.3390/polym16111502
Vorontsov P, Maltseva VY. A review of animal models for bone fracture nonunion and their role in studying biological therapy efficacy. Orthop. Traumatol. Prosthet. [Internet]. 2024; 2:81–87. doi: https://doi.org/qsdc DOI: https://doi.org/10.15674/0030-59872024281-87
Marongiu G, Contini A, Cozzi Lepri A, Donadu M, Verona M, Capone A. The Treatment of Acute Diaphyseal Longbones Fractures with Orthobiologics and Pharmacological Interventions for Bone Healing Enhancement: A Systematic Review of Clinical Evidence. Bioengineering. [Internet]. 2020; 7(1):22. doi: https://doi.org/qsdd DOI: https://doi.org/10.3390/bioengineering7010022
Meiser S, Arora R, Petersen J, Keiler A, Liebensteiner MC, Pallua JD, Wurm A. Radiographic and clinical outcome of tibial plateau fractures treated with bone allograft. Arch. Orthop. Trauma Surg. [Internet]. 2023; 143(5):24472454. doi: https://doi.org/qsdf DOI: https://doi.org/10.1007/s00402-022-04461-x
Bahadoran Z, Mirmiran P, Kashfi K, Ghasemi A. Importance of Systematic Reviews and Meta-analyses of Animal Studies: Challenges for Animal-to-Human Translation. J. Am. Assoc. Lab. Anim. Sci. [Internet]. 2020; 59(5):469-477. doi: https://doi.org/gg637h DOI: https://doi.org/10.30802/AALAS-JAALAS-19-000139
Durmaz B, Gunes N, Koparal M, Gul M, Dundar S, Bingul MB. Investigation of the effects of quercetin and xenograft on the healing of bone defects: An experimental study. J. Oral Biol. Craniofac. Res. [Internet]. 2023; 13(1):22-27. doi: https://doi.org/pmp9 DOI: https://doi.org/10.1016/j.jobcr.2022.10.008